Le cheveu, donc, c’est de la kératine. Mais qu’est-ce cette substance ?
C’est une substance de nature protéique, répondent le chimistes :
- une substance à poids moléculaire élevé contenant des chaînes polypeptidiques qui résultent de la condensation d’acides aminés ; la kératine est une protéine complexe aux nombreuses particularités.
- sa teneur remarquable en soufre, la présence de liaisons de cohésion de divers type expliquent ses propriétés physiques et chimiques étonnantes
En fait, ce terme « kératine » désigne plusieurs individus chimiques différents.

Selon Zviak : « A l’intérieur même du cheveu, plusieurs kératines existent dont la teneur en aminoacides et le comportement chimique peuvent différer. Par exemple, la cuticule résiste à la pepsine alors que le cortex est attaqué. L’on peut aussi démontrer que la kératine de la cuticule a une teneur en soufre plus forte et ceci peut être en corrélation avec cela. Il est égale$ment connu que la kératine de la moelle des cheveux est de loin celle qui est le plus aisément digérée par la trypsine ».
La théorie de H. Thiers
Le professeur H. Thiers a consacré un important chapitre à la kératine dans son ouvrage « les cosmétiques » en voici un extrait :
« Au fur et à mesure que la cellule épidermique évolue vers la surface elle perd sa structure histologique, se dessèche, cesse toute activité vitale et en particulier enzymatique, en même temps qu’elle s’indure : cette « cornification » suivant l’excellent terme proposé par Bekker et King, s’accompagne de l’apparition d’une protéine fibreuse : la kératine.
Les données suivantes ont leurs applications en cosmétique.
Sur le plan chimique, une kératine, comme toute protéine, est formée d’acides aminés : l’intérêt est qu’on y trouve tous les principaux d’entre eux, aussi bien ceux que notre organisme est capable de synthétiser que ceux qualifiés d’essentiels, parce que nous ne pouvons pas les élaborer et devons comme les vitamines et les oligoéléments métalliques les demander au monde extérieur, c’est-à-dire à noter alimentation.
Et comme beaucoup d’esthéticiens » se piquent de conseiller des régimes souvent absurdement insuffisants, il est bon de rappeler au passage que les aliments végétaux sont spécialement pauvres en certains acides aminés essentiels, nécessaires à l’édification de nos protéines.
Par ailleurs, toute kératine est normalement riche en acides aminés soufrés, eux aussi acides aminés essentiels.
Or leur cornification inégale permet d’opposer les structures plus cohérentes et des structures plus lâches ou, si on veut, des kératines dures et des kératines molles.
Plus une structure est indurée, plus sa teneur en cystine l’emporte sur celle en méthionine : la kératinisation est une cystinisation.
Il faut rappeler ici que la source de soufre cutané n’est ni le soufre « précipité lavé, ni les sulfates, ni les hyposulfites : mais le soufre incorporé dans une molécule animée : méthionine ou cystine.
On ne favorise pas la kératinisation en donnant le soufre incorporé dans une autre molécule et l’action thérapeutique du soufre dans les 3 premières formes est indépendante de toute activité kératinisante directe.
Enfin les kératines sont des substances peu réactives donc résistantes, en même temps qu’elles sont douées d’une certaines plasticité qui fait que, si les réactifs chimiques ne sont pas trop agressifs, ils entraînent des modifications permettant un retour à l’état primitif : autre propriété essentielle à l’art de la coiffure.
Bref : richesse en acides aminés essentiels, liaison entre l’état chimique du soufre aminé et l’état physique de la structure kératinisée, inertie mais en même temps relative plasticité permettant le retour à l’état antérieur : voici 3 caractères généraux de la kératine qu’il convient de placer au premier plan en cosmétique ».
La structure physique des kératines en cosmétique présente un intérêt tout spécial. Les kératines sont des protéines fibreuses, c’est-à-dire qu’elles se disposent dans la structure macroscopique qui les contient, en filaments orientés :
- dans le cheveu, c’est suivant le grand axe de l’organe
- dans l’ongle, c’est transversalement
- dans l’épiderme cornée, c’est en sens divers
La kératine
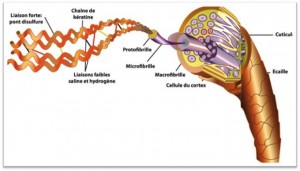
Kératine
La fibre macromoléculaire de la kératine a une architecture pour laquelle nos connaissances sont malheureusement incomplètes.
On distingue 2 types de kératine :
- la kératine dure : celle des cheveux et des ongles
- la kératine molle : celle de la couche cornée de la peau
L’organisation intime, moléculaire, de la kératine dure à pu être révélée grâce aux rayons X. Ils ont montré que les molécules de kératine sont disposées en chaînes longitudinales et parallèles, rattachées les unes aux autres par des « liaisons » ou « ponts » de substances diverses.
Cette disposition donne à l’ensemble l’aspect d’échelles qu’on aurait juxtaposées et dressées verticalement mais dont les barreaux ne seraient pas tous dans le prolongement les uns des autres.
Ainsi :
- les chaînes longitudinales de molécules sont-elles représentées par les montants des échelles
- les « liaison » latérales par les barreaux ou échelons
Ces liaisons sont très importantes puisque, répétons-le ce sont elles qui maintiennent les chaînes et qui donnent à cette architecture sa solidité.
Elles sont de natures très diverses :
- salines
- hydrogénées…
La curiosité des chercheurs a été longtemps retenue par les liaisons dites disulfures, c’est-à-dire constituées par deux atomes de soufre fixés sur une molécule de matière organique appelée cystine.
La cystine
Chimiquement, la cystine est un acide aminé. On nomme acides aminés les constituants fondamentaux des substances protéiques. Il est important de noter dès maintenant que la cystine peut se présenter à l’état de cystéine.
Quelle différence y a-t-il entre ces deux corps ?
- l’un est oxydé
- l’autre est réduit
Rappelons que l’oxydation est un phénomène qui, ramené à ses limites les plus simples, consiste en une fixation d’oxygène, perte d’hydrogène ou addition d’électricité positive;
Le phénomène contraire constitue la réduction.
Ainsi :
- la cystéine si elle cède de l’hydrogène devient la cystine ; c’est une oxydation
- la cystine, si elle fixe de l’hydrogène, devient la cystéine ; c’est une réduction
Lorsque le coiffeur fait une décoloration, il réalise une oxydation intense au niveau de la matière colorante du cheveu par fixation d’oxygène.
Les mèches « coup de soleil » qui se forment naturellement au bord de la mer sont moins l’effet du soleil que d’une oxydation provoquée par l’électricité positive de l’atmosphère, très forte au ras de l’eau.
Revenons à la cystine, dont le symbole S-S rappelle qu’elle porte deux atomes de souffre.
On admet que, des diverses liaisons, c’est elle qui contribue le plus à donner au cheveu son élasticité, et ses propriétés d’élongation.
En outre elle confère à la kératine sa résistance mécanique.
La preuve en est très simple à faire : si l’on coupe les liaisons disulfures, avec un thio, par exemple, le cheveu doivent amorphe, il n’a plus aucune tenue parce que son architecture s’effondre.
L’ennui, c’est que ces liaisons sont assez sensibles à certains produits employés dans le salon de coiffure, les alcalins et les décolorants, en particulier.
N’oubliez pas ce détail car il nous permettra de comprendre les traitements à appliquer aux cheveux décolorés.



